типы химических реакций примеры уравнений реакций 8 класс
типы химических реакций в неорганической химии
типы химических реакций в органической химии
тэги:
8 класс,
примеры уравнений,
химическая реакция,
химия
категория:
образование
ответить
комментировать
в избранное
бонус
1 ответ:
старые выше
новые выше
по рейтингу
0

annamadlen69
[11.8K]
2 недели назад
Химическая реакция — это превращение одних исходных веществ в другие. К химическим реакциям ни в коем случае нельзя отнести процессы изменения агрегатного состояния одного и того же вещества, например образование льда или пара из воды.
В неорганической химии выделяют следующие типы химических реакций:
Реакции соединения. Суть реакции в том, что при взаимодействии двух и более веществ образуется одно новое. В качестве примеров можно привести следующие реакции:
- Fe + S = FeS (взаимодействие порошка серы и порошка железа приведет к образованию сульфида железа).
- С + О2 = СО2 (реакция горения углерода в кислороде с образованием углекислого газа).
- S + О2 = SO2 (реакция горения серы в кислороде с образованием оксида серы IV).
- NH3 + CO2 + H2О = NH4HCO3 (реакция образования гидрокарбоната аммония при взаимодействии аммиака, воды и углекислого газа).
- Na2O + C2O = Na2CO3 (реакция синтеза карбоната натрия путем взаимодействия углекислого газа и оксида натрия).
Реакции разложения. В противоположность реакциям соединения, в реакциях разложения из одного исходного вещества образуется несколько новых. Такие реакции эндотермические, то есть для их протекания необходима энергия извне. Примеры реакций разложения:
-
CaCO3 = CaO + CO2 (реакция разложения карбоната кальция (известняк, мел) на углекислый газ и оксид кальция).
-
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O (разложение соли аммония до молекулярного азота, воды и оксида хрома III).
Реакции обмена. Количество продуктов реакции равно количеству исходных реагентов. Реакции характерны для кислот и оснований. Примеры:
-
HCl + NaOH = NaCl + H2O (соляная кислота и гидроксид натрия при взаимодействии дает соль (хлорид натрия) и воду).
-
Ca(OH)2 + H2SO4 = CaSO4 + 2H2O (гидроксид кальция и соляная кислота дают соль соляной кислоты (сульфат кальция) и воду).
-
KOH + HF = KF + H2O (гидроксид калия и фтористая кислота дают соль фторид калия и воду).
Реакция замещения. Это реакции взаимодействия простого вещества со сложным:
-
Fe + CuSO4 = FeSO4 + Cu (в сульфате меди II железо замещает медь, образуя сульфат железа II).
-
2NaI + Cl2 = 2NaCl + I2 (после взаимодействия хлора из йодида натрия получается хлорид натрия и йод).
В органической химии классификация химических реакций немного иная:
Реакции присоединения. К органической молекуле как правило присоединяются вода, галогены, галогенсодержащие кислоты.
Реакции замещения. Суть реакции замещения в органической химии такая же, как и в неорганической.
Реакция отщепления или элиминирования. В такой реакции от органической молекулы отделяется вещество, как правило неорганическое.
Реакция креккинга, в ходе которой одна органическая молекула распадается на 2 и более молекул, также органических.

Реакция разложения. Суть как и в неорганической химии.
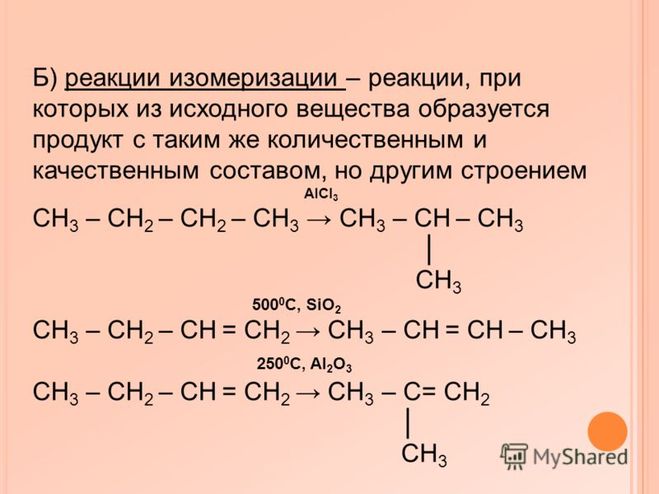
Реакция изомеризации. В органической химии для молекул характерно наличие изомеров. Превращение одного изомера в другой одной и той же молекулы происходит в процессе реакции изомеризации.
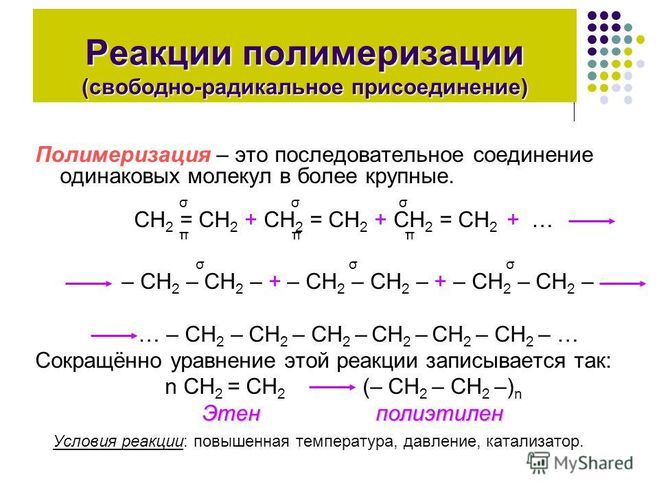
Реакция полимеризации заключается в образовании высокомолекулярного вещества из низкомолекулярного. В биологии полимеризация — очень важный процесс. Ведь белки, ДНК, углеводы — высокомолекулярные вещества, которые путем полимеризации образуются из аминокислот, нуклеотидов и прочих компонентов.
Реакция поликонденсации, продукт которой высокомолекулярное вещество и низкомолекулярное (спирт, вода).
![поликонденсация][4]
комментировать
в избранное
ссылка
отблагодарить
